Actualizado hace 7 minutos
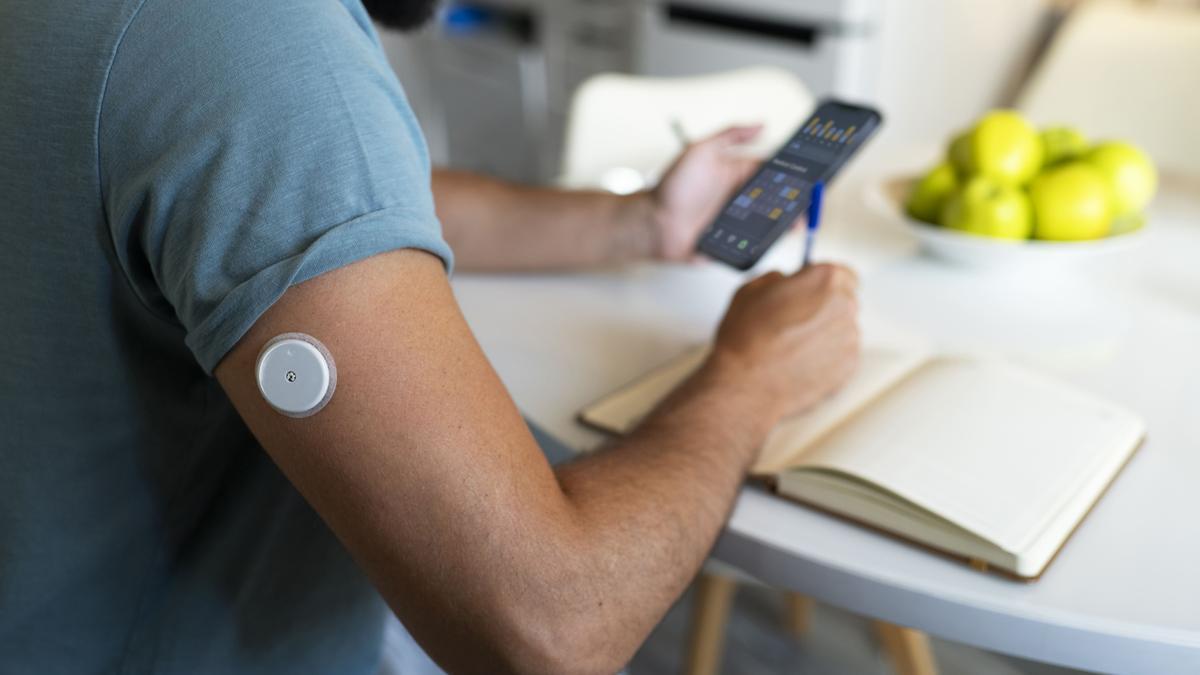
Sanidad ha retirado del mercado un sensor y transmisor del sistema de monitorización continua de glucosa A8 TouchCare System, por errores detectados en un estudio de usabilidad en Portugal, que provocaron varios incidentes.
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha informado que se trata del sensor MD3658 y transmisor MD1158, del fabricante Medtrum Technologies, Inc (China).
Estos productos se han distribuido en el Estado por la empresa Biochemical Systems International S.P.A (Italia), con distribución limitada en un centro en Tenerife, aunque no se descarta su presencia en otros puntos.
Hasta la fecha, la AEMPS no ha recibido notificaciones de incidentes, pero ha adoptado esta medida preventiva, al igual que en Francia y Portugal, a la espera de que el fabricante aporte datos clínicos suficientes que demuestren su seguridad y correcto funcionamiento.
La medida no afecta a la bomba ni al gestor personal de diabetes que forman parte del sistema A8 TouchCare para la administración de insulina y la monitorización de glucosa.
CESE Y RETIRADA DEL PRODUCTO COSMÉTICO
Sanidad también ha ordenado la retirada del producto cosmético Yodeyma Kids, con recuperación de varios lotes en distintos formatos, tras detectarse alérgeno alcohol bencílico en concentración superior al 0,001 %, sin aparecer en el etiquetado.
Los lotes afectados son: EY26KID, EY27KID, EY28KID, EY29KID, EY30KID, EY32KID, EY33KID, EY34KID (125 ml) Y515KID, Y516KID (50 ml) y PY29KID, PY30KID, PY31KID (15 ml).
La AEMPS recuerda que el reglamento establece que los alérgenos deben figurar en el etiquetado si superan el 0,001 %, ya que el uso podría suponer riesgo grave para personas sensibilizadas, siendo relevante en productos destinados a población infantil.
PROHIBICIÓN DEL COMPLEMENTO ALIMENTICIO BICHOTA
Sanidad ha informado del cese de comercialización del producto Bichota, un complemento alimenticio que contiene sildenafilo, principio activo indicado para la disfunción eréctil, en cantidad suficiente para tener condición de medicamento.
La AEMPS tuvo conocimiento, a través del Grupo de Consumo de la Unidad de Delincuencia Especializada y Violenta, de que el producto se comercializaba como complemento alimenticio sin evaluación ni autorización, lo que podría provocar daños graves para la salud. El consumo está contraindicado en pacientes con infarto agudo de miocardio, angina inestable o de esfuerzo, insuficiencia cardiaca, arritmias incontroladas, hipotensión o hipertensión no controlada. Además, presenta numerosas interacciones con otros medicamentos y puede provocar reacciones adversas graves, especialmente de tipo cardiovascular.